अणु सूत्र - NH3
अणुभार - 17
इतिहास (History)
प्राचीन काल में अमोनिया को जानवरों के सींग, खुर आदि के भंजक आसवन द्वारा प्राप्त किया जाता था। 1774 में प्रीस्टले ने इसे नौसादर (अमोनियम क्लोराइड) तथा चूने को एक साथ गर्म करके प्राप्त किया। यह भीगे लाल लिटमस को नीला कर देती है इसलिए उन्होंने इसका नाम क्षारीय वायु (Alkaline air) रखा। नौसादर (Sal-ammoniac) से बनाये जाने के कारण इसका नाम अमोनिया रखा गया।
स्त्रोत (Occurrence)
कुछ मात्रा में यह वायुमण्डल में पायी जाती है। जिन स्थानों पर जीव-जन्तु सड़ते हैं, वहाँ की वायु में इसकी मात्रा अपेक्षाकृत अधिक होती है। प्रकृति में यह अपने लवणों (salts) के रूप में भी पाई जाती है, उदाहरण के लिए- प्रकृति में यह नौसादर (अमोनियम क्लोराइड, NH4CI) तथा अमोनियम सल्फेट [(NH4) 2SO4] के रूप में पाई जाती है। अस्तबलों तथा शौचालयों में तीखी गंध इसी की आती है।
बनाने की विधियाँ (Methods of Preparation)
1. प्रयोगशाला विधि (Laboratory Method) - प्रयोगशाला में अमोनिया, अमोनियम क्लोराइड (नौसादर) को बुझे चुने के साथ गर्म करके बनाई जाती है
2NH4Cl + Ca(OH)2 CaCl2 + 2H2O + 2NH3↑
प्रयोग सामग्री - फ्लास्क, नौसादर, बुझा चूना, निकास नली, स्प्रिट लैम्प आदि।
विधि - एक कठोर काँच की नली में नौसादर (अमोनियम क्लोराइड) और बुझे हुये चूने के मिश्रण को लेकर गर्म किया जाता है। प्राप्त अमोनिया गैस को वायु के अधोमुखी विस्थापन (downward displacement) द्वारा गैस जार में एकत्रित कर लिया जाता है। गैस जार में इकट्ठा करने से पहले इसे अनबुझे चूने (CaO) पर प्रवाहित किया जाता है जिससे इस गैस की नमी दूर हो जाती है।
नोट - अमोनिया को सान्द्र सल्फ्यूरिक अम्ल, अनार्द्र कैल्सियम क्लोराइड या फॉस्फोरस पेण्टा-ऑक्साइड द्वारा नहीं सुखाया जा सकता है क्योंकि अमोनिया इन यौगिकों से रासायनिक अभिक्रियायें कर लेती है।
2NH3 + H2SO4 → (NH4)2SO4
2NH3 + CaCl2 + 2H2O → 2NH4 CI + Ca(OH)2
6NH3 + P2O5 + 3H2O → 2 (NH4)3 PO4
सावधानियाँ- इस प्रक्रिया के दौरान निम्न सावधानियां बरतनी चाहिए-
- गैसजार पूर्णतया सूखा होना चाहिये क्योंकि यह गैस जल में अति विलेय है।
- उपकरण पूर्णतया वायुरोधी होना चाहिए।
- फ्लास्क को धीरे-धीरे तथा समान ऊष्मा द्वारा गर्म करना चाहिये।
- यह गैस वायु से हल्की होती है, इसलिए इसे वायु के अधोमुखी विस्थापन द्वारा एकत्र करना चाहिए।
2. अमोनियम लवण से - अमोनियम लवण को क्षारों के साथ गर्म करने पर अमोनिया प्राप्त होती है। कुछ अमोनियम लवण अकेले गर्म करने पर ही अमोनिया दे देते हैं।
2NH4 Cl + Ca(OH)2 → CaCl2 + 2H2O +2NH3
(NH4)2SO4 + 2NaOH → Na2SO4 + 2H2O + 2NH3
ऊष्मा
(NH4)2SO4 → H2SO4 + 2NH3
3. नाइट्रोजन तथा हाइड्रोजन के संयोग से - उत्प्रेरक की उपस्थिति में लगभग 500°C ताप तथा 200 वायुमण्डलीय दाब पर नाइट्रोजन तथा हाइड्रोजन के संयोग से अमोनिया प्राप्त होती है।
N2 + 3H2 → 2NH3
4. कैल्सियम सायनेमाइड से - कैल्सियम सायनेमाइड पर जल वाष्प की क्रिया से अमोनिया प्राप्त होती है।
CaCN2 + 3H2O → 2NH3 + CaCO3
5. मैग्नीशियम नाइट्राइड पर जल की क्रिया से -
Mg3N2 + 6H2O → 3Mg (OH)2 + 2NH3
6. धात्वीय नाइट्रेटों से - धात्वीय नाइट्रेटों की नवजात हाइड्रोजन से क्रिया से अमोनिया प्राप्त होती है। इस क्रिया में प्रयुक्त नवजात हाइड्रोजन जिंक या ऐलुमिनियम को सोडियम हाइड्रॉक्साइड के साथ गरम करके प्राप्त की जाती है। उदाहरण के लिए-
[Zn + 2NaOH → Na2ZnO2 + 2H] × 4
NaNO3 + 8H → NaOH + 2H2O + NH3
_________________________________________________
4Zn + 7NaOH + NaNO34Na 2 ZnO2 + 2H2O + NH3
5. मैग्नीशियम नाइट्राइड पर जल की क्रिया से -
Mg3N2 + 6H2O → 3Mg (OH)2 + 2NH3
6. धात्वीय नाइट्रेटों से - धात्वीय नाइट्रेटों की नवजात हाइड्रोजन से क्रिया से अमोनिया प्राप्त होती है। इस क्रिया में प्रयुक्त नवजात हाइड्रोजन जिंक या ऐलुमिनियम को सोडियम हाइड्रॉक्साइड के साथ गरम करके प्राप्त की जाती है। उदाहरण के लिए-
[Zn + 2NaOH → Na2ZnO2 + 2H] × 4
NaNO3 + 8H → NaOH + 2H2O + NH3
_________________________________________________
4Zn + 7NaOH + NaNO34Na 2 ZnO2 + 2H2O + NH3
7. कार्बनिक यौगिकों से - कुछ नाइट्रोजन युक्त कार्बनिक यौगिकों को जब सोडा लाइम (NaOH + CaO) के साथ गर्म करते हैं तो अमोनिया प्राप्त होती है। उदाहरण के लिए -
CaO
NH2CONH2 + 2NaOH → Na2CO3 + 2NH3
8. औद्योगिक स्तर पर अमोनियां का निर्माण : हैबर की विधि (Haber's Process) - हैबर ने अमोनिया को व्यापारिक मात्रा में बनाने की विधि का आविष्कार किया, इसलिए इन्हें 1918 में रसायन का नोबेल पुरस्कार प्रदान किया गया। विधि में नाइट्रोजन और हाइड्रोजन आपस में संयोग करके अमोनिया बनाते हैं।
N2 + 3H2 ⇋ 2NH3 + 24,000 कैलोरी
इस क्रिया में ऊष्मा उत्पन्न होती है। यह एक ऊष्माक्षेपी (exothermic) व उत्क्रमणीय (reversible) अभिक्रिया है। इस अभिक्रिया में आयतन में कमी होती है।
हैबर विधि द्वारा अमोनिया के औद्योगिक निर्माण में प्रायः आयरन व मॉलिब्डनम के मिश्रण को उत्प्रेरक के रूप में प्रयुक्त करते हैं। मॉलिब्डनम उत्प्रेरक वर्धक (catalyst promotor) का कार्य करता है।
CaO
NH2CONH2 + 2NaOH → Na2CO3 + 2NH3
8. औद्योगिक स्तर पर अमोनियां का निर्माण : हैबर की विधि (Haber's Process) - हैबर ने अमोनिया को व्यापारिक मात्रा में बनाने की विधि का आविष्कार किया, इसलिए इन्हें 1918 में रसायन का नोबेल पुरस्कार प्रदान किया गया। विधि में नाइट्रोजन और हाइड्रोजन आपस में संयोग करके अमोनिया बनाते हैं।
N2 + 3H2 ⇋ 2NH3 + 24,000 कैलोरी
इस क्रिया में ऊष्मा उत्पन्न होती है। यह एक ऊष्माक्षेपी (exothermic) व उत्क्रमणीय (reversible) अभिक्रिया है। इस अभिक्रिया में आयतन में कमी होती है।
हैबर विधि द्वारा अमोनिया के औद्योगिक निर्माण में प्रायः आयरन व मॉलिब्डनम के मिश्रण को उत्प्रेरक के रूप में प्रयुक्त करते हैं। मॉलिब्डनम उत्प्रेरक वर्धक (catalyst promotor) का कार्य करता है।
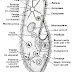
जैसा कि चित्र में दिखाया गया है, वायुमण्डल से प्राप्त नाइट्रोजन गैस तथा भाप अंगार गैस (water gas) से प्राप्त हाइड्रोजन को शुष्क अवस्था में 1 : 3 के अनुपात में मिलाकर 200 वायुमण्डलीय दाब पर एक कक्ष में प्रवाहित किया जाता है, जहाँ पर लगभग 500°C पर उत्प्रेरक रखा होता है। इस कक्ष में ये दोनों गैसें आपस में क्रिया करके अमोनिया बनाती हैं। बची गैसों को पुनः परिसंचारी पम्प (circulatory pump) द्वारा इसी कक्ष में प्रवाहित कर दिया जाता है।
अमोनिया के गुण (Properties of Ammonia)
भौतिक गुण (Physical Properties)
1. यह एक रंगहीन व तीव्र गन्ध वाली गैस है। इसके सूँघने से आँखों से आँसू निकलने लगते हैं। अधिक मात्रा में सूँघने से यह घातक (fatal) भी हो सकती है।
2. अमोनिया का अणु भार 17 तथा वाष्प घनत्व 8.5 है। अतः यह वायु से हल्की है। इसी कारण प्रयोगशाला में इसे वायु के अधोमुखी विस्थापन (downward displacement) द्वारा एकत्रित करते हैं।
3. यह जल में विलेय है। यह जल में अधिक मात्रा में भी घुल जाती है। सामान्य ताप पर इसकी जल में विलेयता 89.9 ग्राम प्रति 100 मि०लि० है। अन्य गैसों की भाँति इसकी जल में विलेयता अधिक ताप पर कम हो जाती है।
4. अमोनिया जल में घुल कर अमोनियम हाइड्रॉक्साइड बनाती है
NH3 + H2O → NH4OH ⇋ NH4+ + OH-
अमोनियम हाइड्रॉक्साइड एक वैद्युत-संयोजी यौगिक है। अतः अमोनिया का जलीय विलयन क्षारीय होता है (लाल लिटमस को नीला कर देता है) तथा विद्युत् का सुचालक है।
5. अमोनिया गैस न स्वयं जलती है और न दूसरे पदार्थों के जलने में सहायक होती है। अमोनिया गैस को वायु में जलाने पर यह नहीं जलती है लेकिन ऑक्सीजन की अधिकता में यह जलने लगती है। अमोनिया गैस के जार में जलती हुई मोमबत्ती ले जाने पर वह बुझ जाती है।
6. अमोनिया का क्रान्तिक ताप 133°C है। अतः सामान्य ताप पर ही दाब बढ़ाते रहने पर यह द्रवित हो जाती है।
रासायनिक गुण (Chemical Properties)
1. जल से अभिक्रिया - यह गीले लाल लिटमस को नीला कर देती है इसलिए इसका जलीय विलयन क्षारीय होता है।
NH3 + H2O → NH4OH ⇋ NH+ + OH-
2. क्षारीय गुण - यह अम्लों से अभिक्रिया करके लवण बनाती है।
2NH3 + H2SO4 → (NH4)2 SO4
NH3 + HCl → NH4Cl
NH3 + HNO3 → NH4NO3
3. दहन - अमोनिया न स्वयं जलती है न दूसरे पदार्थों के जलने में सहायक होती है। ऑक्सीजन की अधिकता में यह पीली लो के साथ जलती है।
4NH3 +3O2 → 6H2O+ 2N2
अमोनिया तथा ऑक्सीजन गैस के मिश्रण को 800°C पर प्लैटिनम की गरम जाली पर से प्रवाहित करने पर नाइट्रिक ऑक्साइड (NO) तथा जल प्राप्त होते हैं।
800°C
4NH3+5O2 → 4NO + 6H2O
4. ऊष्मीय अपघटन - अमोनिया एक स्थायी यौगिक है लेकिन उच्च ताप पर या विद्युत्-स्फुलिंग (electric spark) प्रवाहित करने पर यह अपने अवयवों में वियोजित हो जाती है।
2NH3 → N2 + 3H2
5. इलोजेनों से क्रिया - यदि अमोनिया की अधिक मात्रा की क्रिया क्लोरीन की कम मात्रा से कराई जाये तो नाइट्रोजन गैस बनती है।
2NH3 + 3Cl2 → N2 + 6HCI
6NH3 + 6HCI → 6NH4CI
_____________________________
3NH3 + 3Cl2 → N2 + 6NH4 Cl
यदि क्लोरीन की अधिक मात्रा की क्रिया अमोनिया की कम मात्रा से करायी जाती है तो नाइट्रोजन ट्राइ क्लोराइड (NCI3) बनता है जो एक अति विस्फोटक पदार्थ है।
3Cl2 + NH3 → NCI3 + 3HCL
अमोनिया की ब्रोमीन से क्रिया होने पर भी नाइट्रोजन गैस ही बनती है।
2NH3 + 3Br2 → N2 + 6HBr
6NH3 + 6HBr → 6NH4Br
_____________________________
8NH3 +3Br2 → N2 + 6NH4Br
यह आयोडीन के साथ क्रिया करके एक काले रंग का विस्फोटक पदार्थ (NI3) बनाती है।
3I2 + 4NH3 → NI3 + 3NH4I
अमोनिया की जल में विलेयता
अमोनिया की जल में विलयता निम्न प्रयोग द्वारा समझाई जा सकती है -
प्रयोग - एक गोल पेंदी वाले फ्लास्क में शुष्क अमोनिया लेते हैं जिसमें कॉर्क की सहायता से टोंटीदार निकास नली लगाते हैं। इस फ्लास्का को स्टैण्ड में उल्टा कस देते हैं। निकास नली का सिरा जल से भरी नाद में डूबा रहता है। जल में लाल लिटमस का विलयन मिला होता है। निकास नली में लगी स्टॉप कॉर्क को खोलने पर जल फ्लाक्स में फव्वारे की भाँति जाने लगता है। अनोनिया गैस लाल लिटमस विलयन को नीला कर देती है। इस प्रकार फ्लाक्स में जाकर जल का रंग नीला हो जाता है। नाँद से भरे जल का तेजी से फ्लाक्स में जाना अनोनिया की जल में अधिक विलेयता को प्रदर्शित करता है।
8NH3 +3Br2 → N2 + 6NH4Br
यह आयोडीन के साथ क्रिया करके एक काले रंग का विस्फोटक पदार्थ (NI3) बनाती है।
3I2 + 4NH3 → NI3 + 3NH4I
अमोनिया की जल में विलेयता
अमोनिया की जल में विलयता निम्न प्रयोग द्वारा समझाई जा सकती है -
प्रयोग - एक गोल पेंदी वाले फ्लास्क में शुष्क अमोनिया लेते हैं जिसमें कॉर्क की सहायता से टोंटीदार निकास नली लगाते हैं। इस फ्लास्का को स्टैण्ड में उल्टा कस देते हैं। निकास नली का सिरा जल से भरी नाद में डूबा रहता है। जल में लाल लिटमस का विलयन मिला होता है। निकास नली में लगी स्टॉप कॉर्क को खोलने पर जल फ्लाक्स में फव्वारे की भाँति जाने लगता है। अनोनिया गैस लाल लिटमस विलयन को नीला कर देती है। इस प्रकार फ्लाक्स में जाकर जल का रंग नीला हो जाता है। नाँद से भरे जल का तेजी से फ्लाक्स में जाना अनोनिया की जल में अधिक विलेयता को प्रदर्शित करता है।
उपयोग (Uses)
- इसे बर्फ बनाने के कारखानों में शीतलक के रूप में प्रयोग करते हैं।
- इसका जलीय घोल (NH4OH) प्रयोगशाला में एक प्रमुख अभिकर्मक के रूप में प्रयुक्त होता है।
- इसकी सहायता से विभिन्न अमोनियम लवण बनाये जाते हैं जो कृत्रिम खाद तथा औषधियों के रूप में प्रयोग में आते हैं।
- इसका प्रयोग कृत्रिम रेशे बनाने में होता है।
- इसका उपयोग अश्रु गैस बनाने में होता है।
परीक्षण (Tests)
- अमोनिया गैस से भरे गैस जार के मुँह पर हाइड्रोक्लोरिक अम्ल (HCI) से भीगी छड़ ले जाने पर अमोनियम क्लोराइड (NH4Cl) का सफेद धुंआ निकलता है।
- भीगा हुआ लाल लिटमस नीला हो जाता है।
- इसकी गन्ध तीव्र तथा आँसू लाने वाली होती है।
%20%20%E0%A4%87%E0%A4%A4%E0%A4%BF%E0%A4%B9%E0%A4%BE%E0%A4%B8,%20%E0%A4%AC%E0%A4%A8%E0%A4%BE%E0%A4%A8%E0%A5%87%20%E0%A4%95%E0%A5%80%20%E0%A4%B5%E0%A4%BF%E0%A4%A7%E0%A4%BF,%20%E0%A4%97%E0%A5%81%E0%A4%A3,%20%E0%A4%89%E0%A4%AA%E0%A4%AF%E0%A5%8B%E0%A4%97,%20%E0%A4%AA%E0%A4%B0%E0%A5%80%E0%A4%95%E0%A5%8D%E0%A4%B7%E0%A4%A3.webp)



No comments:
Post a Comment