सल्फर डाइ-ऑक्साइड (Sulphur di-Oxide)
%20%20%E0%A4%87%E0%A4%A4%E0%A4%BF%E0%A4%B9%E0%A4%BE%E0%A4%B8,%20%E0%A4%B8%E0%A5%8D%E0%A4%A4%E0%A5%8D%E0%A4%B0%E0%A5%8B%E0%A4%A4,%20%E0%A4%AC%E0%A4%A8%E0%A4%BE%E0%A4%A8%E0%A5%87%20%E0%A4%95%E0%A5%80%20%E0%A4%B5%E0%A4%BF%E0%A4%A7%E0%A4%BF,%20%E0%A4%97%E0%A5%81%E0%A4%A3.webp)
अणु सूत्र - SO2
अणु भार - 64
इतिहास (History)
प्राचीन समय में गन्धक (sulphur) के जलने से उत्पन्न धुएँ का कीटाणुनाशक के रूप में उपयोग किया जाता था। गंधक के जलने से जो गैस बनती है वह सल्फर डाइ-ऑक्साइड होती है। सबसे पहले रसायनज्ञ प्रीस्टले ने सन् 1774 ई० में इस गैस को पारे पर सान्द्र सल्फ्यूरिक अम्ल के साथ गर्म करके बनाया था। प्रीस्टले ने इस गैस का नाम कसीस की वायु (Vitrolic air) रखा। सन् 1777 ई० में लेवोसिये ने गंधक को वायु में जलाकर सल्फर डाइ-ऑक्साइड को प्राप्त किया।स्रोत (Occurrence)
सल्फर डाइ-ऑक्साइड ज्वालामुखी पर्वतों से निकलने वाली गैसों में उपस्थित होती है। यह ज्वालामुखी पर्वतों के आस-पास के झरनों में बहुत अधिक मात्रा में पायी जाती है। कुछ मात्रा में यह नगरों की वायु में भी पाई जाती है जो कि कोयले में मिले गंधक तथा इसके यौगिकों के जलने पर प्राप्त होती है।बनाने की विधि (Methods of Preparation)
1. प्रयोगशाला विधि (Laboratory Method) - प्रयोगशाला में सल्फर डाइ-ऑक्साइड गैस, ताँबे की छीलन को सान्द्र सल्फ्यूरिक अम्ल के साथ गर्म करके प्राप्त की जाती है।
Cu + 2H2SO 4 → CuSO4 + 2H2O + SO2
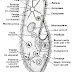
विधि - एक गोल पेंदी के फ्लास्क में ताँबे की कुछ छीलन लेते हैं। इस फ्लास्क के मुँह पर दो छेद वाली कॉर्क लगाते हैं। एक छेद में थिसिल नली तथा दूसरे छेद में समकोण में मुड़ी हुई निकास नली लगाते हैं। एक अन्य फ्लास्क में सान्द्र सल्फ्यूरिक अम्ल लेकर उसमें भी दो छेद वाला कॉर्क, लगाते हैं। पहले फ्लास्क में लगी निकास नली का दूसरा सिरा दूसरे फ्लास्क में लगे कॉर्क के पहले छेद में से होकर फ्लास्क में भरे सल्फ्यूरिक अम्ल में दूबो दिया जाता है।
कॉर्क के दूसरे छेद में एक अन्य समकोण में मुड़ी निकास नली लगाते हैं। इस निकास नली का दूसरा सिरा गैसजार में लगाया जाता है। अब थिसिल कीप से इतना सान्द्र H2SO4 फ्लास्क में डालते हैं कि कीप का निचला सिरा अम्ल में डूब जाये। फ्लास्क को बर्नर की सहायता से गर्म करके सल्फर डाइऑक्साइड गैस बनायी जाती है। अब इसे सान्द्र H2SO4 से भरे फ्लास्क में पहुँचाया जाता है। वहाँ इसकी नमी को अम्ल द्वारा शोषित कर लिया जाता है तथा इस शुष्क गैस को वायु के उर्ध्व विस्थापन द्वारा एकत्र कर लिया जाता है। सल्फर डाइऑक्साइड गैस से गैस जार भरा है या नहीं इसका पता लगाने के लिये गीले लिटमस पेपर को गैस जार के मुँह पर ले जाते हैं। यदि लिटमस पेपर लाल हो जाता है तो इसका मतलब है कि गैसजार में सल्फर डाइ-ऑक्साइड भरी है।
सावधानियाँ-
(i) फ्लास्क को धीरे-धीरे गर्म करना चाहिए।
(ii) SO2 जल में विलेय है इसलिये गैस जार सूखा होना चाहिये।
(iii) उपकरण वायुरोधी होने चाहिये।
(iv) थिसिल कीप का निचला सिरा अम्ल में डूबा रहना चाहिये।
2. जब सल्फर को वायु में जलाया जाता है तो सल्फर डाइऑक्साइड प्राप्त होती है।
S + O2 → SO2
Cu + 2H2SO4 → CuSO4 + 2H2O + SO2
Hg + 2H2SO4 → HgSO 4 + 2H2O + SO2
S + 2H2SO4 → 2H2O + 3SO2
C + 2H2SO4 → 2H2O + CO2 + 2SO2
सल्फर डाइ-ऑक्साइड के गुणधर्म
भौतिक गुण (Physical Properties)(1) यह एक रंगहीन, तीव्र गंध वाली पारदर्शक गैस है।
(2) यह गला घोटने वाली विषैली गैस होती है।
(3) यह वायु से भारी होती है। इसका वाष्प घनत्व 32 है।
(4) यह जल में विलेय है।
(5) यह हिम मिश्रण में ठंडा किये जाने पर एक रंगहीन द्रव में परिवर्तित हो जाती है जिसका क्वथनांक- 10°C है।
रासायनिक गुण (Chemical Properties)
(1) जल से क्रिया - जल में घुलकर यह सल्फ्यूरस अम्ल (H2SO3) बनाती है। अतः इसका जलीय घोल अम्लीय होता है। यह नीले लिटमस को लाल कर देता है।
H2O + SO2 → H2SO3
(2) अम्लीय गुण - यह क्षारों के साथ क्रिया करके लवण बनाती है। उदाहरण के लिए-
(3) अपघटन - सूर्य के प्रकाश की उपस्थिति में या 1200°C पर यह अपघटित होकर सल्फर तथा सल्फर ट्राइ-ऑक्साइड (SO3) गैस बनाती है।
2NaOH + SO2 → Na2SO3 + H2O
(3) अपघटन - सूर्य के प्रकाश की उपस्थिति में या 1200°C पर यह अपघटित होकर सल्फर तथा सल्फर ट्राइ-ऑक्साइड (SO3) गैस बनाती है।
3SO2 → S↓ + 2SO3↑
(4) क्लोरीन से अभिक्रिया - क्लोरीन से अभिक्रिया करके यह योगात्मक यौगिक सल्फ्यूरिल क्लोराइड (SO2Cl2 )
SO2 + Cl2 → SO2Cl2
Pt (उत्प्रेरक)
2SO2 + O2 → 2SO3
450°C
(6) अपचायक गुण - (i) जलीय विलयन में यह फेरिक क्लोराइड (FeCl3) को फेरस क्लोराइड में अपचयित कर देती है।
FeCl3 + 2H2O + SO2 → 2FeCl 2 + 2HCl + H2SO4
K2Cr2O7 + H2SO4 + 3SO2 → K2SO4 + Cr2(SO4)3 + H2O
2KMnO4 + 5SO2 + 2H2O → K2SO4 + 2MnSO4 + 2H2SO4
(7) ऑक्सीकारक गुण
यह H2S को S में ऑक्सीकृत कर देती है।
SO2 + 2H2S → 3S↓ + 2H2O
PbO2 + SO2 → PbSO4
(8) विरंजक गुण - यह गैस भीगे हुए रंगीन फूल-पत्तियों आदि का रंग उड़ा देती है। विरंजन की क्रिया इस प्रकार होती है।
SO2 + H2O → H2SO3
H2SO3 + H2O → H2SO4 + 2H (नवजात हाइड्रोजन)
रंगीन पदार्थ + H → रंगहीन पदार्थ
FAQs
1. सल्फर डाइ-ऑक्साइड का प्रमुख स्रोत कौन सा है?
Ans. सल्फर डाइऑक्साइड कई स्रोतों द्वारा उत्पन्न होते हैं जिनमें शामिल हैं:
- ज्वालामुखी विस्फोट और ज्वालामुखी गैसें: ज्वालामुखी विस्फोट के दौरान भारी मात्रा में सल्फर डाइऑक्साइड (SO₂) वायुमंडल में छोड़ी जाती है।
- जीवाश्म ईंधनों का दहन करने पर: कोयला और तेल जैसे जीवाश्म ईंधनों को जलाने पर SO₂ उत्पन्न होता है। यह बिजली संयंत्रों, औद्योगिक प्रतिष्ठानों और वाहनों से निकलने वाले धुएं का एक प्रमुख घटक होती है।
- धातुकर्म: धातुओं के निष्कर्षण और शोधन की प्रक्रियाओं में सल्फर यौगिकों का उपयोग किया जाता है, जिससे SO₂ का उत्सर्जन होता हैं।
- अन्य स्रोतों द्वारा: कई अन्य प्रौद्योगिकी प्रक्रियाएं भी हैं जैसे जैव ईंधन का दहन, जंगलों की आग। इनके द्वारा भी वातावरण में SO₂ उत्सर्जन होता हैं।
2. सल्फर डाइ-ऑक्साइड का रासायनिक सूत्र क्या है?
Ans. सल्फर डाइऑक्साइड का रासायनिक सूत्र SO₂ है।
3. सल्फर डाइ-ऑक्साइड का रंग कैसा होता हैं?
Ans. यह एक रंगहीन गैस है।
4. सल्फर डाइ-ऑक्साइड सबसे अधिक कहाँ पाया जाता हैं?
Ans. यह गैस सबसे अधिक वायुमंडल में पाया जाता है। यहाँ यह प्राकृतिक और मानवीय गतिविधियों दोनों से उत्पन्न होता है।
5. क्या सल्फर डाइ-ऑक्साइड गैस जहरीली हैं?
Ans. हाँ, सल्फर डाइऑक्साइड एक जहरीली गैस है। यह श्वसन तंत्र को परेशान कर सकती है, जिससे सांस लेने में तकलीफ, खांसी, सीने में दर्द और गले में जलन जैसी समस्या हो सकती हैं।
Related article-


No comments:
Post a Comment