कोशिका में ऊर्जा ग्राही (वाहक) [Energy Acceptors (Carriers) in the Cell]
कोशिका में ऊर्जाक्षेपी (exergonic) क्रियाओं में मुक्त ऊर्जा को कुछ यौगिक ग्रहण करते हैं। इन्हें ऊर्जा ग्राही। (energy carriers) कहते हैं। इनके विघटन से मुक्त ऊर्जा फिर ऊर्जाशोषी (endergonic) क्रियाओं में प्रयुक्त होती है। कोशिका में में प्रमुख ऊर्जा ग्राही यौगिक निम्नलिखित हैं
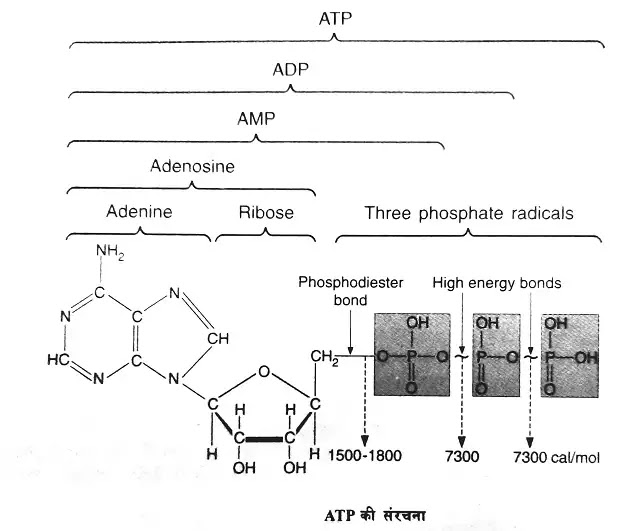
(i) एडीनोसीन ट्राइफॉस्फेट ( ATP)
कोशिका में एडीनोसीन ट्राइफॉस्फेट (ATP) मुक्त ऊर्जा को ग्रहण करने वाला मुख्य पदार्थ है। यह एक न्यूक्लिओटाइड (nucleotide) होता है जिसमें एडीनोसीन (adenosine) नामक न्यूक्लिओसाइड (nucleoside) के साथ तीन फॉस्फेट समूह जुड़े होते हैं।
एडीनोसीन का निर्माण एडीनीन बेस (adenine base) तथा राइबोस शर्करा (ribose sugar) के मिलने से होता है। एडीनोसीन के साथ एक फॉस्फेट समूह जुड़ने से एडीनोसीन मोनोफॉस्फेट (AMP) बनता है। फॉस्फेट का यह समूह कम ऊर्जा वाले बन्ध (bond) द्वारा जुड़ता है। इस बन्ध में 1500-1800 cal/mol ऊर्जा संचित रहती है। इस बन्ध को सीधी रेखा (-) से प्रदर्शित करते हैं।
एडीनोसीन मोनोफॉस्फेट के साथ दूसरा फॉस्फेट समूह जुड़ने से एडीनोसीन डाइफॉस्फेट (ADP) बनता है। एडीनोसीन डाइफॉस्फेट के साथ तीसरा फॉस्फेट समूह जुड़ने से एडीनोसीन ट्राइफॉस्फेट (ATP) का निर्माण होता है। दूसरे व तीसरे फॉस्फेट समूह उच्च ऊर्जा वाले बन्धों (high energy bonds) द्वारा जुड़ते हैं। इन बन्धों को सिगमॉयड (sigmoid) वक्र ' ~ ' द्वारा प्रदर्शित किया जाता है। उच्च ऊर्जा बन्धों के निर्माण के लिए अधिक ऊर्जा की आवश्यकता होती है। प्रत्येक उच्च ऊर्जा वाले बन्ध (high energy bond) के टूटने से 7300 कैलोरी प्रति मोल ऊर्जा मुक्त होती है।
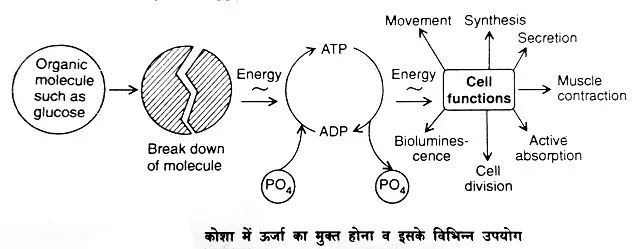
कोशिका में लगभग 90% ATP माइटोकॉण्ड्रिया में संग्रहित रहती है। यहीं पर ATP ADP में परिवर्तन होता रहता है। कार्बनिक पदार्थों, विशेष रूप से ग्लूकोस के ऑक्सीकरण से ऊर्जा मुक्त होती है। यह मुक्त ऊर्जा तुरन्त ही विभिन्न क्रियाओं में प्रयुक्त नहीं होती, बल्कि पहले ADP व फॉस्फेट समूह के संयोजन से ATP में संचित हो जाती है। आवश्यकता के समय ATP का उच्च ऊर्जा वाला बन्ध (~) टूट जाता है, इससे फॉस्फेट समूह अलग हो जाता है तथा ADP बनता है।
इस बन्ध के टूटने से मुक्त ऊर्जा विभिन्न क्रियाओं में प्रयुक्त होती रहती है। इससे स्पष्ट है कि ATP की "बन्ध ऊर्जा" (bond energy) ही जैव-ऊर्जा (bio-energy) है।
इस प्रकार कोशिका में ऊर्जाक्षेपी (exergonic) क्रियाओं व ऊर्जाशोषी (endergonic) क्रियाओं के बीच ADP का ATP में संगठन तथा ATP का ADP में विघटन चक्र चलता रहता है। इसे ही कोशिका में ऊर्जा चक्र (energy cycle) कहते हैं। ATP को कोशिका में ऊर्जा की मुद्रा (currency of energy) भी कहते हैं।
(ii) क्रिएटिन फॉस्फेट (Creatine Phosphate)
पेशी कोशिकाओं में क्रिएटिन फॉस्फेट नामक ऊर्जा ग्राही पदार्थ होता है। पेशी के विश्रामावस्था में अनॉक्सीय दशा में ATP, क्रिएटिन से क्रिया करके क्रिएटिन फॉस्फेट बनाती है।
ATP + Creatine ⇌ ADP + Pi + Creatine ⇌ ADP + Creatine Phosphate
पेशी के संकुचन के समय क्रिएटिन फॉस्फेट विघटित हो जाता है और मुक्त ऊर्जा पुनः ATP में संचित हो जाती है।
(iii) अन्य ऊर्जा-ग्राही यौगिक (Other Energy Carrier Compounds)
श्वसन क्रिया में भाग लेने वाले कुछ यौगिक, जैसे फॉस्फोइनोल पाइरुविक अम्ल, 1,3- डाइफॉस्फोग्लिसरिक अम्ल, ऐसीटिल कोएन्जाइम-A, आदि उच्च ऊर्जा युक्त फॉस्फेट बन्ध यौगिक हैं, इनके अतिरिक्त कोशिका में अन्य ऊर्जा युक्त यौगिक भी होते हैं, जैसे ग्वानीन ट्राइफॉस्फेट (GTP), यूरिडीन ट्राइफॉस्फेट (UTP), आर्जिनीन फॉस्फेट (arginine phosphate), साइटीडाइन ट्राइफॉस्फेट (CTP), कार्बोमिल फॉस्फेट (carbamyl phosphate), कार्बोक्सिलिक अम्ल (carboxylic acid), आदि। ये सभी पदार्थ विभिन्न उपापचयी क्रियाओं (metabolic reactions) में महत्त्वपूर्ण कार्य करते हैं।
कोशिका में इलेक्ट्रॉन-संवाहक (Electron Carriers in the Cell)
जीवित कोशिकाओं में होने वाली कुछ उपापचयी क्रियाओं में मुक्त हाइड्रोजन परमाणु (2H) प्रोटॉन्स (2H+) व इलेक्ट्रॉन्स (2e-) में टूट जाते हैं। हाइड्रोजन परमाणु के इन इलेक्ट्रॉन्स में विभव ऊर्जा (potential energy) संग्रहित होती है।
मुक्त इलेक्ट्रॉन्स फिर कुछ यौगिकों, जिन्हें संवाहक (carriers) कहते हैं, से होकर गुजरते हैं। इससे ऑक्सीकरण (oxidation) तथा अपचयन (reduction) क्रियाएँ होती हैं। इलेक्ट्रॉन्स के संवाहक से मुक्त होने पर ऑक्सीकरण तथा दूसरे संवाहक (carriers) पर पहुँचने पर अपचयन होता है। इस प्रकार इलेक्ट्रॉन प्राप्तकर्ता (oxidant) तथा इलेक्ट्रॉन दाता (reductant) साथ-साथ रहते हैं। इन्हें रेडॉक्स युगल (Redox couple) कहते हैं। इलेक्ट्रॉन्स के संवाहकों (carriers) से होकर गुजरने को इलेक्ट्रॉन परिवहन तन्त्र (electron transport system) कहते हैं। इस क्रिया में ऊर्जा मुक्त होती है जो ATP के रूप में संचित हो जाती है।
इलेक्ट्रॉन परिवहन तन्त्र में ऑक्सीजन (O2) अन्तिम इलेक्ट्रॉन प्राप्तकर्ता होती है। यह अन्त में इलेक्ट्रॉन (e) तथा प्रोटॉन (H) को लेकर जल का निर्माण करती है। कोशिका की निम्न क्रियाओं में विभिन्न इलेक्ट्रॉन-संवाहक (electron carriers) भाग लेते हैं।
(1) कोशिकीय श्वसन (Cellular respiration) – कोशिकीय श्वसन में ग्लाइकोलाइसिस (glycolysis) तथा क्रैस चक्र (Krebs' cycle) में विभिन्न कार्बनिक पदार्थों से हाइड्रोजन मुक्त होती है। यह इलेक्ट्रॉन व प्रोटॉन में टूट जाती है। माइटोकॉण्ड्रिया के क्रिस्टी (cristae) पर इलेक्ट्रॉन-संवाहकों (electron carriers) की एक शृंखला होती है। मुक्त इलेक्ट्रॉन इसी श्रृंखला से होकर गुजरते हैं और इससे मुक्त ऊर्जा ATP में संचित होती है। इस क्रिया में निम्न इलेक्ट्रॉन संवाहक भाग लेते हैं—
(a) NAD+ (Nicotinamide Adenine Dinucleotide) —यह प्रथम इलेक्ट्रॉन-संवाहक है। NAD+ एक डाइन्यूक्लिओटाइड है जिसमें एक न्यूक्लिओटाइड का निर्माण एडीनीन, राइबोस शर्करा तथा फॉस्फेट समूह से होता है तथा दूसरे न्यूक्लिओटाइड में निकोटिनेमाइड, राइबोस शर्करा तथा फॉस्फेट समूह होता है। दोनों न्यूक्लिओटाइड्स के फॉस्फेट समूह परस्पर जुड़े रहते हैं। अतः NAD+ की संरचना निम्न है-
Adenine Nicotinamide
| |
Ribose Ribose
| |
Phosphate —— Phosphate
NAD+ एक कोएन्जाइम (coenzyme) है जो एन्जाइम अभिक्रिया में भाग लेता है। यह ग्लाइकोलाइसिस व क्रैब्स चक्र से हाइड्रोजन लेकर अपचयित अवस्था NADH में आ जाता है। NADH अणु दो इलेक्ट्रॉन्स (2e-) तथा एक प्रोटोन (H+) खोकर पुनः NAD+ में उपचयित (oxidised) हो जाता है।
NAD+ + 2H+ + 2e- ⇌ NADH + H+ or NAD.2H or NADH2
NAD.2H के एक अणु से ATP के तीन अणुओं की प्राप्ति होती हैं।
(b) FAD (Flavin Adenine Dinucleotide) - यह दूसरा प्रमुख इलेक्ट्रॉन-संवाहक (electron carrier) है। यह राइबोफ्लेविन या विटामिन B2 से उत्पन्न होता है। इसकी संरचना निम्न प्रकार है
Isoalloxazine ring Adenine
| |
Ribitol Ribose
| |
Phosphate —— Phosphate
इसकी संरचना में एक न्यूक्लिओटाइड में राइबोस के स्थान पर राइबिटॉल होता है। अतः वास्तव में इस भाग को न्यूक्लिओटाइड नहीं कहा जा सकता। NAD+ के विपरीत FAD एक प्रोस्थेटिक समूह है, जो एपोएन्जाइम (apoenzyme) के साथ स्थायी रूप से जुड़ा रहता है। यह दो हाइड्रोजन परमाणुओं को प्राप्त करके FADH2 में बदलता है।
FAD + 2H+ + 2e- ⇌ FAD.H2
प्रत्येक FAD.2H अणु से 2 इलेक्ट्रॉन तथा 2 हाइड्रोजन परमाणु निकलकर ऑक्सीजन तक पहुँचने के क्रम में 2 ATP अणुओं का संश्लेषण होता है।
(c) कोएन्जाइम Q (Coenzyme Q = CoQ या Ubiquinone) - यह इलेक्ट्रॉन-संवाहक किसी प्रोटीन से सम्बद्ध नहीं होता और माइटोकॉण्ड्रिया की झिल्ली पर स्वतन्त्र रूप से गति करता है। यह वसा में घुलनशील होता है तथा इलेक्ट्रॉन-संवाहक (electron carrier) होने के साथ ही यह प्रोटॉन भी ग्रहण करता है। यह दो इलेक्ट्रॉन्स के स्थान अगले संवाहक को केवल एक इलेक्ट्रॉन स्थानान्तरित (transfer) करता है।
(d) साइटोक्रोम्स (Cytochromes) — इन इलेक्ट्रॉन-संवाहकों में हीम (heme) एक प्रोस्थेटिक समूह (prosthetic group) के रूप में होता है। ये प्रायः लाल रंग के होते हैं। ये अनेक प्रकार के होते हैं तथा शृंखला में भाग लेने के क्रम में क्रमशः साइटोक्रोम, b, c, a व a3 हैं। ये संवाहक जब इलेक्ट्रॉन प्राप्त करते हैं या शृंखला में इलेक्ट्रॉन अगले संवाहक को स्थानान्तरित करते हैं तो Fe अणु Fe2+ तथा Fe3+ अवस्था के बीच दोलन (oscillate) करते रहते हैं।
विभिन्न साइटोक्रोम्स में साइटोक्रोम - c सबसे छोटा प्रोटीन अणु होता है जिसमें केवल 100 ऐमीनो अम्ल होते हैं। यह माइटोकॉण्ड्रिया की भीतरी झिल्ली पर ढीले रूप से (loosely) संलग्न रहता है और पृथक् होकर स्वतन्त्र रूप से गति कर सकता है।
(2) हेक्सोस मोनोफॉस्फेट शन्ट (Hexose Monophosphate Shunt - HMS) - यह ऑक्सी- श्वसन (aerobic respiration) की क्रिया-विधि का दूसरा विकल्प है। यह क्रिया परिपक्व पादप कोशाओं (mature plant cells) के cytoplasm में होती है। यकृत कोशाओं (livercells) में कुल श्वसन का 60% इसी विधि से होता है। इस क्रिया में ग्लूकोस के ऑक्सीकरण से मुक्त ऊर्जा व हाइड्रोजन द्वारा NADPH) का निर्माण होता है। इस यौगिक के ऑक्सीकरण से इलेक्ट्रॉन्स मुक्त होते हैं जो ऑक्सीजन (O2) को अपचयित (reduce) कर देते हैं तथा मुक्त ऊर्जा ATP में संचित हो जाती है।
(3) प्रकाश-संश्लेषण (Photosynthesis) - प्रकाश संश्लेषण की प्रकाश अभिक्रिया (light reaction) के प्रकाश-कर्म I में सूर्य के प्रकाश के फोटोन (photon), पर्णहरिम-a (Pigment-700) से टकराते हैं। फोटोन की क्वाण्टम (quantum) ऊर्जा को अवशोषित करके पर्णहरिम - a से अधिक ऊर्जा वाले चार इलेक्ट्रॉन्स निष्कासित होते हैं। इसी प्रकार प्रकाश कर्म II में भी पर्णहरिम-a (Pigment 680) से अधिक ऊर्जा वाले चार इलेक्ट्रॉन्स मुक्त होते हैं। दोनों प्रकाश-कर्मों में मुक्त इलेक्ट्रॉन्स फिर अनेक संवाहकों, जैसे - प्रकाश क्रम I में आइरन सल्फर प्रोटीन ग्राही (AFeS), फेरीडॉक्सिन (Fd) FAD, NADP तथा प्रकाश क्रम II में फियोफाइटिन (Pheo), प्लास्टोक्विनॉन (PQ), साइटोक्रोम b6-f, प्लास्टोसायनिन (PC), आदि से होकर गुजरते हैं। इस क्रिया में मुक्त ऊर्जा ATP के रूप में संचित हो जाती है।
(4) जैविक नाइट्रोजन यौगिकीकरण में इलेक्ट्रॉन-प्रवाह (Flow of Electron in Biological Nitrogen Fixation) — डाइनाइट्रोजन (dinitrogen, N2) के मध्य स्थित त्रि-बन्ध (N≡N) बहुत स्थायी होने के कारण इनका अपचयन (reduction) सरलता से सम्भव नहीं होता है। औद्योगिक संस्थानों में डाइनाइट्रोजन के मध्य के तीनों बन्धों का अपचयन (reduction) उच्च ताप एवं उच्च दाब पर ही सम्भव है। डाइनाइट्रोजन के जैविक अपचयन (biological reduction) के लिये भी आश्रित पौधों (host plants) द्वारा प्रकाश संश्लेषण से प्राप्त पदार्थों (photo assimilates) की काफी मात्रा में आवश्यकता पड़ती है।
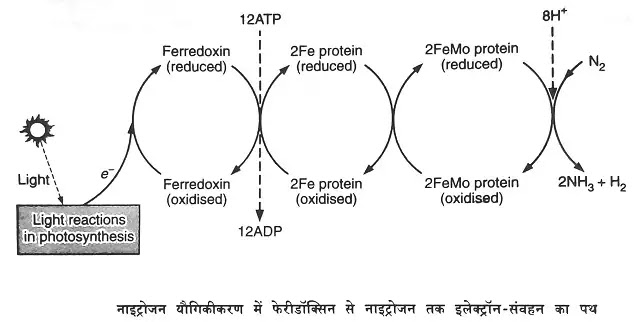
भूमि में सहजीवी पौधों (symbiotic plants) में नाइट्रोजन स्थिरीकरण (nitrogen fixation) की क्रिया डाइनाइट्रोजिनेस (dinitrogenase) एन्जाइम द्वारा उत्प्रेरित (catalysed) होती है। यह क्रिया भूमि में स्थित प्रोकैरियोट्स (prokaryotes) द्वारा ही सम्भव होती है, क्योंकि इस क्रिया के लिये आवश्यक विकरों (enzymes) के जीन केवल प्रोकैरियोट्स में ही होते हैं। डाइनाइट्रोजिनेस विकर (dinitrogenase enzyme) विभिन्न आकार (different size) की दो उपइकाइयों (subunits) का बना होता है। इनमें छोटा प्रोटीन एक डाइमर (dimer) है जिसमें एक समान (identical) पॉलिपेप्टाइड (polypeptide ) दो उपइकाइयाँ (subunits) होती हैं। पॉलिपेप्टाइड की दोनों उपइकाइयों (subunits) का अणु भार जीवाणु की जाति के आधार पर 24 से 36kD के बीच होता है। इसमें नॉन-हीम (non-heme) लौह होता है। इसे Fe प्रोटीन (Fe protein) अथवा डाइनाइट्रोजिनेस रिडक्टेस (dinitrogenase reductase) कहते हैं। इसके डाइमर (dimer) में चार आइरन आयन (four iron ions) चार सल्फर समूह (four sulphur groups) से जुड़े रहते हैं (FeaSa)। डाइनाइट्रोजिनेस विकर ( dinitrogenase enzyme) के बड़े भाग को MoFe protein कहते हैं। यह एक चतुष्क (tetramer) है, जिसमें एक समान (identical), पॉलिपेप्टाइड (polypeptide) की दो उपइकाइयों (subunits) के दो जोड़े (two pairs) होते हैं। जिनका अणु भार (molecular weight) लगभग 220 kD होता है। प्रत्येक MoFe प्रोटीन अणु में दो मॉलिब्डेनम आयन (two molybdenum ions) आइरन मॉलिब्डेनम सल्फर सहकारक (iron-molybdenum sulphur cofactor) के रूप में रहते हैं। MoFe protein में थोड़ी मात्रा में Fe4S4 समूह भी होता है, यद्यपि इसकी वास्तविक मात्रा (exact number) की जानकारी अभी तक ज्ञात नहीं है। इसकी मात्रा स्पीशीज के कार्य (function of species) अथवा इसकी शरीरक्रियात्मक स्थिति (physiological condition) पर निर्भर करती है। डाइनाइट्रोजन (N2) के अमोनिया (NH3) में अपचयन (reduction) के लिये दोनों ही घटक अनिवार्य हैं। डाइनाइट्रोजिनेस रिडक्टेस (dinitrogenase reductase) के सक्रियण (activation) के लिये आवश्यक ऊर्जा ATP से प्राप्त होती है।
जैविक नाइट्रोजन यौगिकीकरण (biological nitrogen fixation) में नाइट्रोजन (N2) का अपचयन (reduction) नाइट्रोजिनेस विकर द्वारा अमोनिया (NH) में होता है।
सहजीवी पौधों (symbiotic plants) में अवशोषित नाइट्रोजन (N2) का अमोनिया (NH3) में परिवर्तन दो चरणों में होता है—
प्रथम चरण (first step) में Fe प्रोटीन का इलेक्ट्रॉन दाता (electron donor) फेरीडॉक्सिन (ferredoxin) द्वारा अपचयन (reduction) हो जाता है। फेरीडॉक्सिन (ferredoxin) नाइट्रोजन यौगिकीकरण (nitrogen fixation) के अतिरिक्त प्रकाश-संश्लेषण क्रिया में भी इलेक्ट्रॉन-संवाहक (electron carrier) के रूप में कार्य करते हैं।
द्वितीय चरण (second step) में अपचयित Fe प्रोटीन (reduced Fe protein) अपना इलेक्ट्रॉन FeMo प्रोटीन नाइट्रेट रिडक्टेस को देकर उपचयित (oxidised) हो जाता है। अपचयित FeMo प्रोटीन डाइनाइट्रोजन गैस (N) एवं हाइड्रोजन (H2) दोनों के अपचयन (reduction) को उत्प्रेरित (catalysed) करता है। जिससे नाइट्रोजन का अमोनिया (NH3) में अपचयन (reduction) हो जाता है।
%20(1).webp)


No comments:
Post a Comment